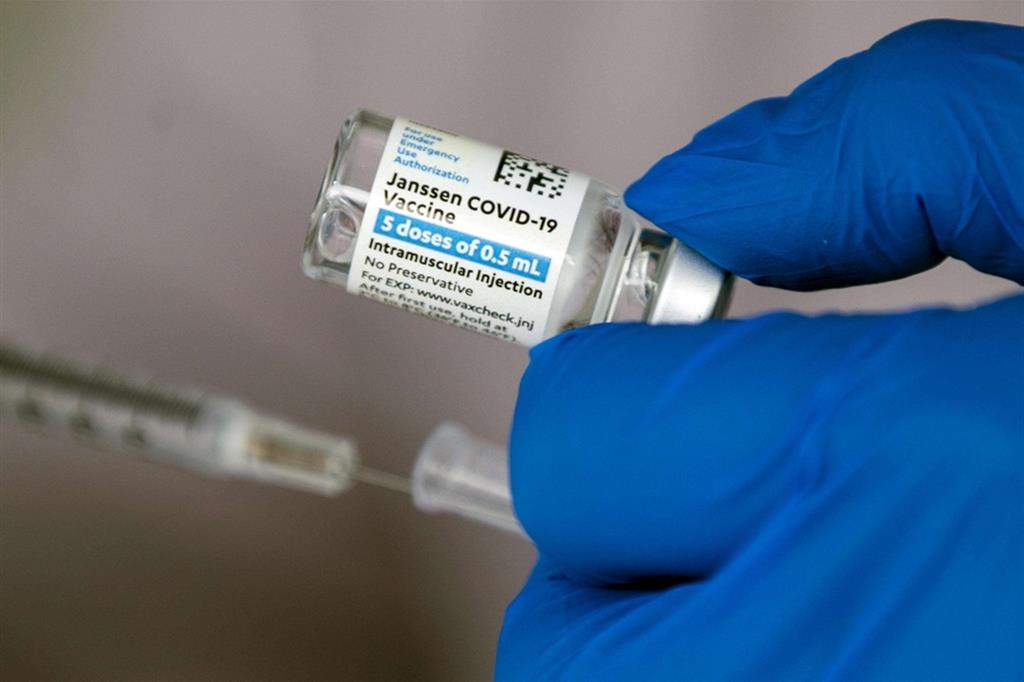
Ansa
L'azienda farmaceutica americana Johnson&Johnson ha annunciato che ritarderà le consegne all'Europa dopo che gli Stati Uniti hanno sospeso oggi il suo vaccino anti Covid, Janssen, in attesa di luce su alcuni casi di coagulazione.
"Come misura precauzionale, raccomandiamo una pausa dell'uso del vaccino", scrive su Twitter la Food & Drug Administration, l'agenzia Usa per i farmaci. La notizia arriva nel giorno dello sbarco in Italia delle prime dosi del vaccino di J&J, l'unico monodose, sul quale si conta nei prossimi mesi per accelerare la campagna vaccinale. Il ministro della Salute, Roberto Speranza, ha convocato per questo pomeriggio una riunione con i vertici dell'Agenzia italiana del farmaco (Aifa).
E la Johnson & Johnson, che ha consegnato oggi le sue prime dosi di vaccino anti-Covid anche in Europa, precisa, dopo quanto deciso in America, di aver deciso di "ritardare il lancio" del proprio siero nel vecchio continente, "in un'ottica di trasparenza e in attesa delle valutazioni delle autorità sanitarie europee".
Le autorità sanitarie statunitensi, Cdc e Fda, in una conferenza stampa, questo pomeriggio hanno fatto sapere che la sospensione del vaccino Johnson&Johnson sarà probabilmente una questione di giorni. "Quello che vediamo per i vaccini Johnson&Johnson è simile a quanto osservato con AstraZeneca". Lo
affermano le autorità sanitarie americane nel corso di un incontro per spiegare perché hanno raccomandato una pausa nella somministrazione del vaccino per il Covid di J&J. I problemi con il vaccino Johnson&Johnson si hanno in media nove giorni dopo lasomministrazione.
Stop Usa dopo 6 casi di trombosi, uno letale
Negli Usa da oggi i centri vaccinali gestiti dal governo federale (Centers for Disease Control) interromperanno l'uso del vaccino, mentre la misura viene presentata come una raccomandazione per le autorità sanitarie che fanno capo ai singoli stati. Le autorità federali, comunque, si aspettano che gli Stati seguano il loro esempio.
La sospensione, informa il New York Times, è legata ai casi di sei vaccinati negli Stati Uniti che hanno sviluppato una malattia rara che coinvolge coaguli di sangue nelle due settimane successive alla somministrazione. Si tratta esclusivamente di donne giovani, tra i 18 ed i 48 anni. Una è morta e un'altra è ricoverata in gravi condizioni in Nebraska. Non è chiaro se queste trombosi rare siano uguali a quelle che potrebbero essere causate dal vaccino di AstraZeneca.
Sono quasi sette milioni gli statunitensi immunizzati con J&J e altre nove milioni di dose sono state esportate all'estero. "Siamo consapevoli che eventi tromboembolici, compresi quelli con trombocitopenia, sono stati segnalati con vaccini contro il Covid-19", afferma J&J in una dichiarazione, aggiungendo però che "al momento non è stato dimostrato nessun nesso causale chiaro fra questi eventi rari e il vaccino Janssen" contro il coronavirus.
Il coordinatore della Casa Bianca per la risposta al Covid, Jeff Zients, ha dichiarato che lo stop deciso "per eccesso di prudenza dall'Fda e dai Cdc non avrà un impatto significativo sul nostro piano vaccinale". Sarà rispettato, ha assicurato, "l'obiettivo del presidente di 200 milioni di dosi entro i suoi primi giorni di incarico".
Johnson & Jonhnson ha anche spiegato che le autorità sanitarie Usa hanno messo a disposizione informazioni sul corretto riconoscimento e gestione di questi disturbi a causa del trattamento unico richiesto da questo tipo di coaguli di sangue. Le autorità sanitarie, precisa l'azienda, "consigliano alle persone che hanno ricevuto il nostro vaccino contro il Covid-19 e che sviluppano un forte mal di testa, dolore addominale, dolore alle gambe o respiro corto entro tre settimane dalla vaccinazione di contattare il proprio medico".
Le prime dosi J&J in Italia, restano in magazzino
In Italia dove sono arrivate nel pomeriggio, all'hub nazionale della Difesa di Pratica di Mare, le prime 184mila dosi del vaccino Janssen della Johnson & Johnson, quindi, questi vaccini rimarranno "stoccati" in attesa delle verifiche. "Nei nostri container le dosi possono essere conservate fino a due anni, c'è tutto il tempo per gli accertamenti del caso", ha spiegato a Rainews 24 Stefano Sbaccanti, della struttura commissariale per l'emergenza Covid. "La campagna vaccinale prosegue - ha aggiunto - ci sono aumenti rispetto alle prime stime, tutte le dosi che arrivano andranno alle Regioni".
In una nota del commissario straordinario all'emergenza Francesco Paolo Figliuolo si legge che "nella tarda serata di ieri sono state inoltre consegnate circa 175mila dosi di vaccino Vaxzevria (di AstraZeneca, ndr). I due arrivi sono parte dei 4,2 milioni di dosi che giungeranno in Italia nel periodo 15-22 aprile, che, assieme a quelle nelle disponibilità delle Regioni, contribuiranno in modo significativo al raggiungimento del target della campagna a livello nazionale".
Il vaccino Janssen, di J&J, è il quarto approvato dall'Ema, l'agenzia europea per i farmaci, dopo Pfizer, Moderna e Vaxzevria di AstraZeneca.
Intanto in Italia sono stati superati i 4 milioni di cittadini immunizzati con due dosi contro il Covid, secondo i dati sul sito del governo. All'ultimo aggiornamento delle 17.10 sono esattamente 4.018.236.
Speranza: valutazioni in corso
Il ministro della Salute, Roberto Speranza prova a rassicurare: "Valuteremo nei prossimi giorni il da farsi, ma Johnson&Johnson resta un vaccino importante da usare". "Abbiamo fatto oggi una riunione con i nostri scienziati e l'Aifa e siamo in collegamento con l'Ema - speiga - decideremo, appena Ema e gli Usa ci daranno notizie più definitive, quale sarà la strada migliore".
Astrazeneca, nota dell'Aifa per i medici: vigilare sui segni
Gli operatori sanitari "devono vigilare su segni e sintomi di tromboembolia e/o trombocitopenia e informare di conseguenza i vaccinati". Lo afferma l'Aifa nella "Nota informativa importante" sul vaccino anti-Covid di
AstraZeneca Vaxzevria, pubblicata a seguito della procedura condotta a livello europeo. La Nota aggiorna gli operatori sanitari sui punti emersi dalla valutazione del vaccino. Una relazione causale tra la vaccinazione con Vaxzevria e l'insorgenza di trombosi in combinazione con trombocitopenia, afferma Aifa, è considerata "plausibile".
In questa fase, precisa l'Agenzia italiana del farmaco, non sono stati identificati fattori di rischio specifici. "La segnalazione di reazioni avverse sospette dopo l'autorizzazione del medicinale è importante, inquanto - si legge nella Nota - consente il monitoraggio continuo del rapporto beneficio/rischio di questo e di qualsiasi altro medicinale. Si ricorda, pertanto, agli operatori sanitari di continuare a segnalare le sospette reazioni avverse associate all'uso di Vaxzevria, in conformità con il sistema nazionale di segnalazione spontanea". Questo medicinale, rileva l'Aifa, "è soggetto a monitoraggio addizionale. Ciò consente una rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta".










.jpg?dt=1735205342850&Width=300)
.jpg?dt=1735205342850&width=677)